Bakgrunn og studiedesign
Retatrutide (LY3437943) er et nytt enkeltpeptidlegemiddel som aktiverertre reseptorer samtidigGIP, GLP-1 og glukagon. For å evaluere effekt og sikkerhet hos personer med fedme, men uten diabetes, ble det utført en randomisert, dobbeltblind, placebokontrollert fase 2-studie (NCT04881760). Totalt338 deltakeremed en BMI ≥30, eller ≥27 med minst én vektrelatert komorbiditet, ble randomisert til å motta placebo eller retatrutid (1 mg, 4 mg med to titreringsplaner, 8 mg med to titreringsplaner, eller 12 mg) administrert én gang ukentlig ved subkutan injeksjon i 48 uker.primært endepunktvar den prosentvise endringen i kroppsvekt ved 24 uker, med sekundære endepunkter inkludert vektendring ved 48 uker og kategoriske vekttapsterskler (≥5 %, ≥10 %, ≥15 %).
Viktige resultater
-
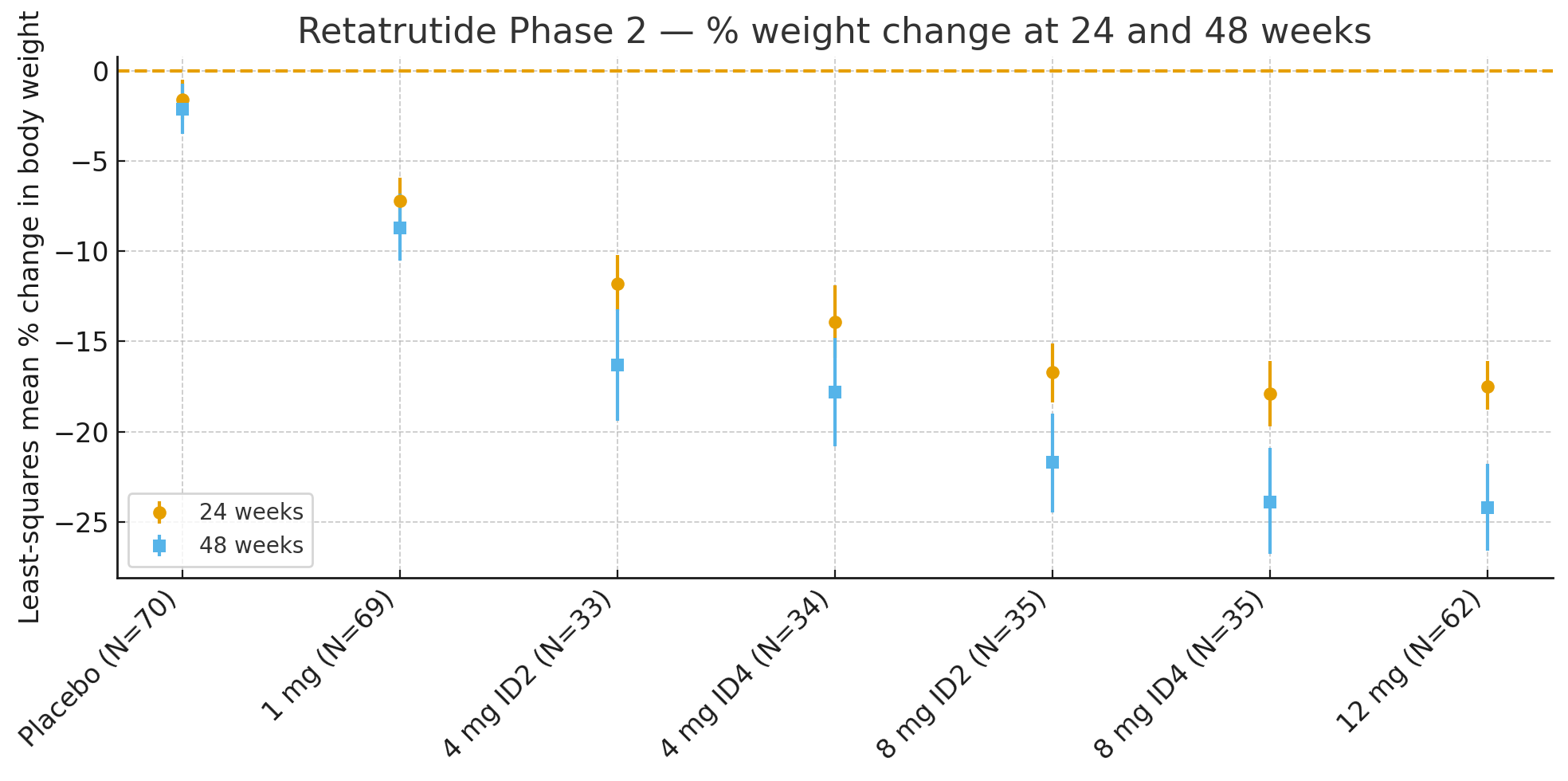
24 ukerMinste kvadraters gjennomsnittlige prosentvise endring i kroppsvekt i forhold til baseline var
-
Placebo: −1,6 %
-
1 mg: −7,2 %
-
4 mg (kombinert): −12,9 %
-
8 mg (kombinert): −17,3 %
-
12 mg: −17,5 %
-
-
48 ukerProsentvis endring i kroppsvekt var
-
Placebo: −2,1 %
-
1 mg: −8,7 %
-
4 mg (kombinert): −17,1 %
-
8 mg (kombinert): −22,8 %
-
12 mg: −24,2 %
-
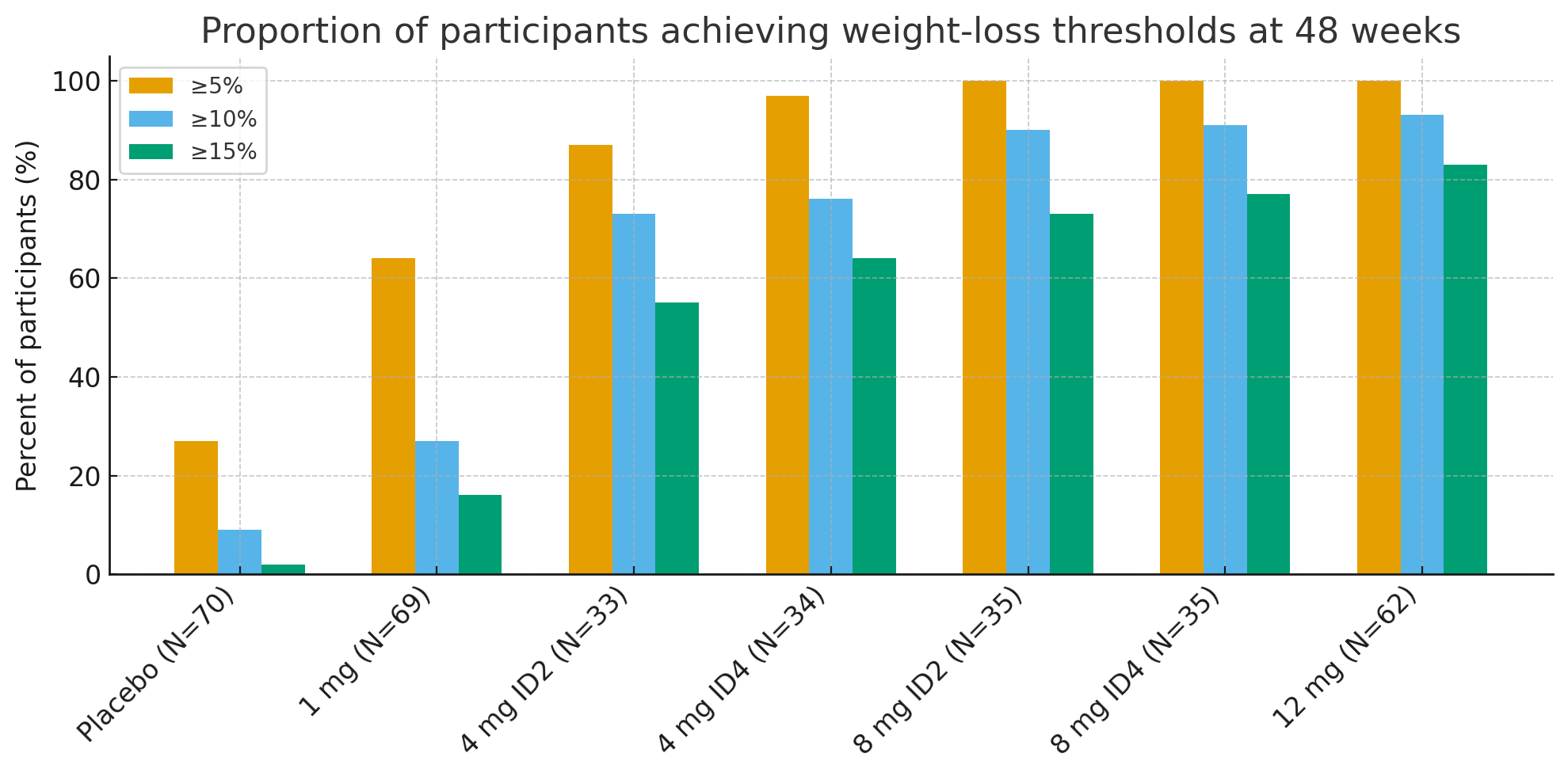
Etter 48 uker var andelen deltakere som oppnådde klinisk meningsfulle vekttapsterskler slående:
-
≥5 % vekttap: 27 % med placebo vs. 92–100 % i aktive grupper
-
≥10 %: 9 % med placebo vs. 73–93 % i aktive grupper
-
≥15 %: 2 % med placebo vs. 55–83 % i aktive grupper
I 12 mg-gruppen, opptil26 % av deltakerne mistet ≥30 % av sin opprinnelige vekt, en størrelsesorden av vekttap som kan sammenlignes med fedmekirurgi.
Sikkerhet
De vanligste bivirkningene var gastrointestinale (kvalme, oppkast, diaré), vanligvis milde til moderate og doserelaterte. Lavere startdoser (2 mg titrering) reduserte disse hendelsene. Doserelaterte økninger i hjertefrekvens ble observert, med en topp i uke 24, deretter avtagende. Seponeringsraten varierte fra 6–16 % på tvers av aktive grupper, noe høyere enn placebo.
Konklusjoner
Hos voksne med fedme uten diabetes produserte ukentlig subkutan retatrutid i 48 ukerbetydelige, doseavhengige reduksjoner i kroppsvekt(opptil ~24 % gjennomsnittlig tap ved høyeste dose), sammen med forbedringer i kardiometabolske markører. Gastrointestinale bivirkninger var hyppige, men håndterbare med titrering. Disse fase 2-funnene tyder på at retatrutid kan representere en ny terapeutisk referanse for fedme, i påvente av bekreftelse i større, langsiktige fase 3-studier.
Publisert: 28. september 2025